cis-trans光異性化について
cis体とtrans体の熱平衡
単結合の場合、結合は自由に回転できるため、分子は複数の立体配座をとり得ます。これに$\pi$結合が加わって二重結合になると結合が自由に回転できなくなり、cis体とtrans体という2種類の異性体「ジアステレオマー」(diastereomer) が生じます。
※高校の教科書などには未だに「幾何異性体」(geometrical isomer) という名称で紹介されているかもしれませんが、現在ではこの名称は推奨されておらず、より広い定義を持つジアステレオマーという名称が推奨されています。
例えば2-ブテンには、中央の二重結合によりcis体とtrans体という2種類のジアステレオマーが存在しています。
 図.2-ブテンのジアステレオマー
図.2-ブテンのジアステレオマー
単結合の回転に要する活性化エネルギーは通常、高々数十[kJ/mol]程度であり、その活性化障壁は室温で十分に越えることができます。一方で二重結合が回転するためには数百[kJ/mol]程度という大きなエネルギーを必要とするため、室温の範囲では活性化障壁を越えることができず、cis体とtrans体が相互に変換することはありません。
例えば2-ブテンの場合では二重結合の回転に240[kJ/mol]程度のエネルギーを要することが量子化学計算(以下はDFT計算の結果)から求められます。一般に室温において越えられる活性化障壁の高さがおよそ100[kJ/mol]程度であることを考えると、cis体とtrans体の互変異性は起こらないことが分かります。
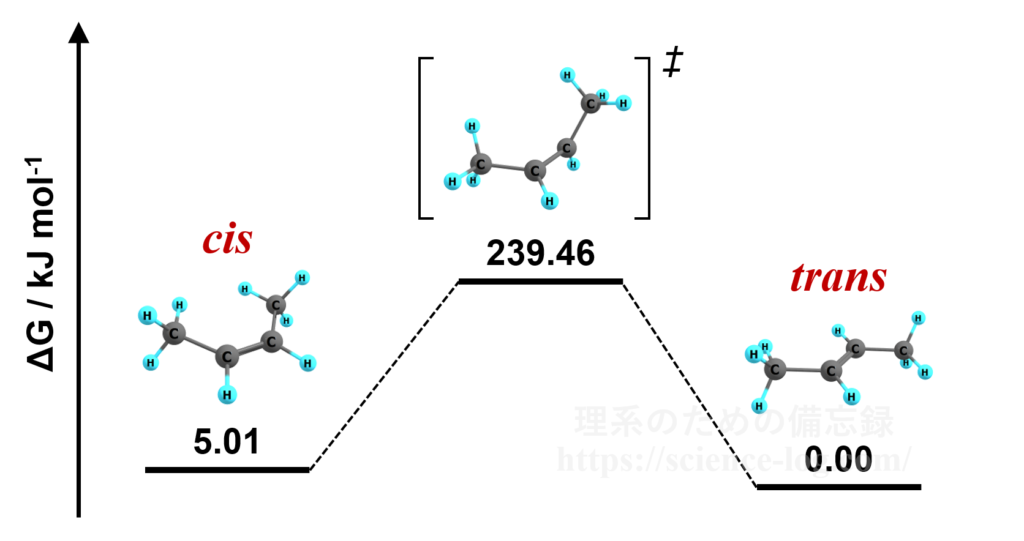 図.2-ブテンの異性化のエネルギーダイアグラム
図.2-ブテンの異性化のエネルギーダイアグラム
(縦軸はB3LYP/6-31+G*レベルの計算で求めた自由エネルギー)
cis-trans光異性化
上記のように、cis-transの異性化には$\pi$結合の切断に伴う大きな活性化障壁が存在するため、特殊な実験条件でもない限り2種類のジアステレオマーが相互に行ったり来たりすることはありません。
高い活性化障壁を越えさせる最も単純な方法は、反応系を生成系よりも高エネルギー、つまりエネルギー的に(熱力学的に)不安定な状態にすることです。
そのためには幾つかの方法が考えられますが、一番手っ取り早いのが「加熱」です。反応器を加熱することで系中の分子にエネルギーを与え、活性化障壁を超えられるだけのエネルギーを持った分子の数を増やすのです。有機化学の実験でも反応系を加熱して反応を進めることがありますよね。
もう一つの方法が「光照射」です。多くの化学反応は基底状態と呼ばれる最も安定な電子配置をとる状態の下で進行しますが、ある特定の波長をもつ光(電磁波)を反応系に照射して分子にエネルギーを与えることで、より高いエネルギーをもった電子配置の状態「励起状態」を作り出すことができます。これにより反応の舞台となるポテンシャルエネルギー面を変えて反応経路そのものを改変し、基底状態では実現しえないような反応経路を辿らせることができるのです。
分子によって吸収できる光(電磁波)の波長の長さは決まっており、励起状態に遷移させるにはちょうどよい特定の波長を照射する必要があります。例えば、cis体のスチルベンに紫外光(270~280[nm])を照射して励起させると $\textrm{C=C}$ 結合まわりに捻じれて、約1ピコ秒のタイムスケールでtrans体へと異性化することが知られています。
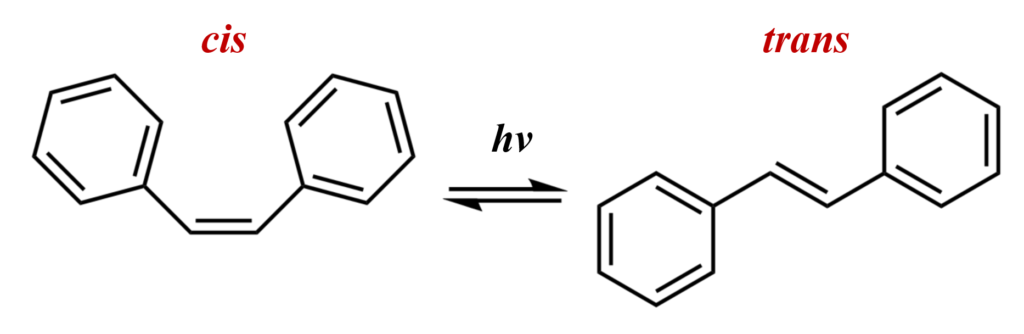 図.スチルベンの光異性化
図.スチルベンの光異性化
スチルベンのcis-trans異性化の活性化エネルギーは480[kJ/mol]以上と非常に大きいのですが、光照射によって分子を励起させて大きなエネルギーを注入することで、光異性化を誘発することができます。
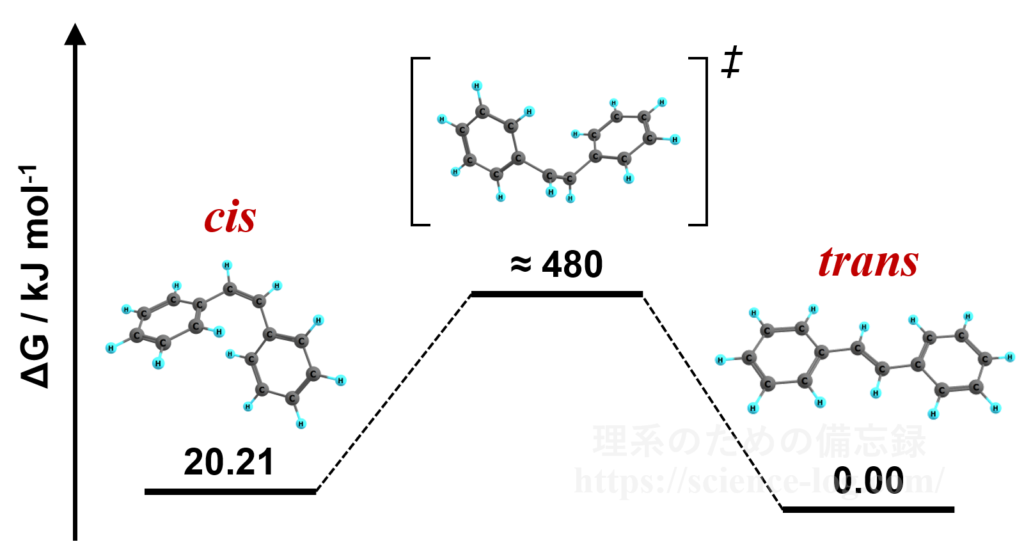 図.スチルベンの異性化のエネルギーダイアグラム
図.スチルベンの異性化のエネルギーダイアグラム
(縦軸はB3LYP/6-31+G*レベルの計算で求めた自由エネルギー)
光異性化の機構
光異性化の機構を理解するにはエネルギーポテンシャル面がイメージできるとスムーズです。それぞれの電子状態におけるエネルギーは分子の構造(座標)に対して決まっており、電子状態によって「安定な構造」が異なります。この「安定な構造」というのは基底状態の分子だけでなく、励起状態における分子の安定な構造も含んでいます。
以下の図は、基底状態$\mathrm{S_0}$のcis体のスチルベン分子を励起させたときのエネルギーポテンシャル面の模式図です。
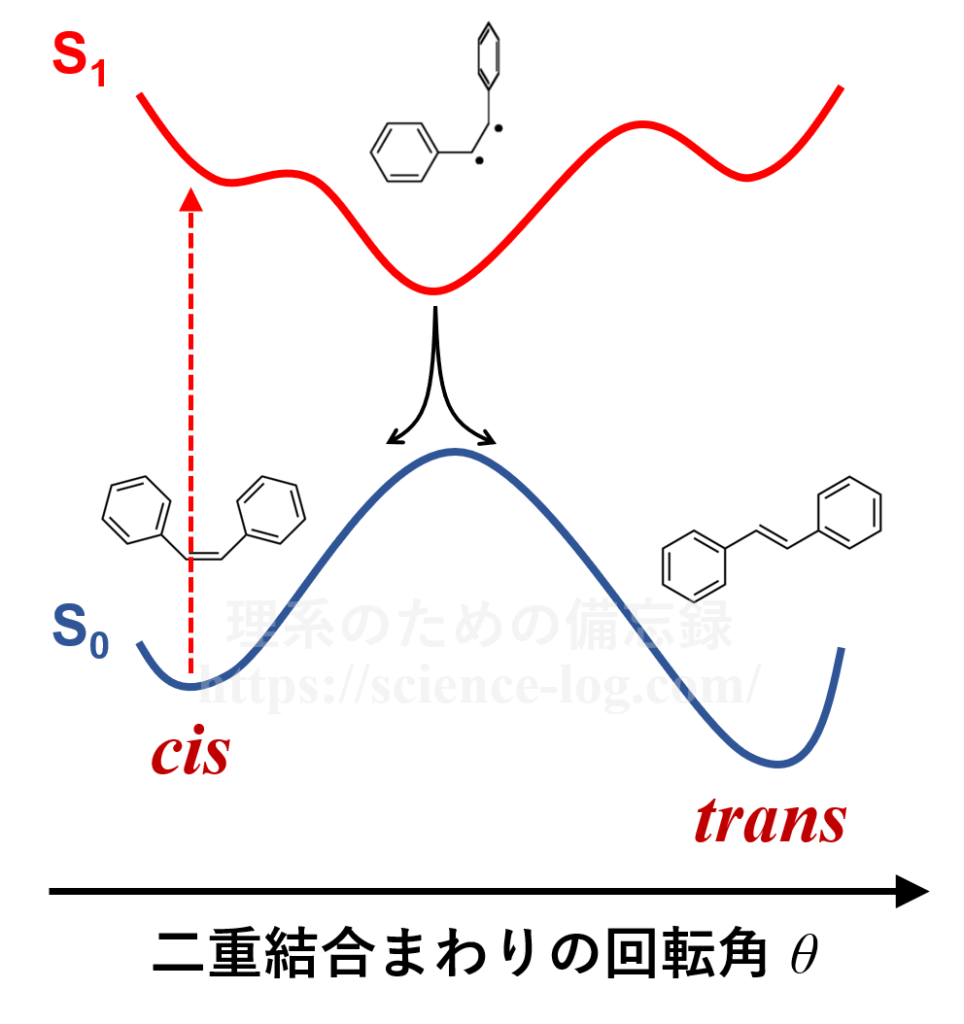 図.スチルベン分子のポテンシャル面
図.スチルベン分子のポテンシャル面
基底状態$\mathrm{S_0}$のcis体のスチルベン分子に対して紫外光を照射すると最低励起一重項状態($\mathrm{S_1}$状態)へと遷移し、$\mathrm{S_1}$状態におけるエネルギー極小構造へと速やかに緩和します。この構造が$\mathrm{S_0}$状態における $\textrm{C=C}$ 結合回転の遷移状態に近いため、基底状態に失活した分子の一部がtrans体へと異性化するのです。
cis-スチルベンの吸収極大が約276[nm]、trans-スチルベンの吸収極大が約294[nm]と近く、吸収バンドもブロードであるため、cis体だけを狙って励起させることはできません。$\mathrm{S_1}$状態におけるエネルギー地形ではcis-trans変異の遷移状態付近の構造($\textrm{C-Ph}$ 結合が直角の構造)でエネルギー極小となるため、$\mathrm{S_0}$状態に失活した分子の一部はcis体に戻り、一部はtrans体に向かいます。
$\pi$結合の切断を伴う二重結合の回転によるcis-trans光異性化は、このような反応機構によって起こります。こうした光を用いて誘起される化学反応を光化学反応(または光反応)と呼び、光による物性の発現や変化を調べる分野は光化学と呼ばれ、現在世界中で盛んに研究されています。
