大学の有機化学:立体化学を知る(不斉炭素編)
$\require{mhchem}$
✎不斉炭素をおさらい
本節からはいよいよ立体化学を本格的に扱っていきます。まずは
「不斉炭素」(ふせいたんそ)
について軽く復習しましょう。詳しく知りたい方は「【高校化学】不斉って何?不斉炭素原子とは?」のページをご覧下さい!
不斉というのは英語で “asymmetry” を意味し「対称でない」ということを表しています。有機化学で頻繫に登場する不斉炭素とは、4つの結合手が異なる原子または置換基と共有結合しているような炭素を指します。

この図のように、4方向の結合相手がすべて異なるような炭素を不斉炭素と言い、4方向の結合相手がすべて異なるような原子を不斉中心と呼びます。
主にこうした不斉炭素により、分子には「立体配置」の概念が付きまとうのです。
✎鏡の中の分子?
まずは簡単な(?)クイズから。以下の図を見て下さい。
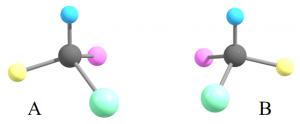
AとBという2つの分子があります。同じ色の球は同種の原子だとすると、AとBは同じ分子でしょうか?それとも異なる分子でしょうか?
・・・皆さんお分かりでしょうが、これらの分子は互いに「鏡写し」の関係にあります。このように組成は等しくても立体配置が異なるような分子は互いに異性体と呼ばれます。特に、こうした鏡写しの関係にあるものを鏡像異性体と言い、一般に「エナンチオマー」と称されます。
AとBの分子はどんなに頑張って重ね合わせても互いに一致することはありません。この関係はまるで左右対称な左手と右手の関係のようです。

これに準えて、このような関係は「掌性」(しょうせい)、若しくは「対掌性」(たいしょうせい)と呼ばれます(対称性ではないので注意!)。これを英語では “chirality” (キラリティ)と呼び、掌性をもつことを「キラル」(chiral)であると言います。また、逆に掌性をもたないことは「アキラル」(achiral)であると言います。
よくあるキラリティの導入材料の一つに乳酸があります。
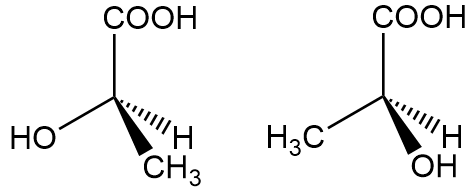
乳酸分子の中心の炭素から生えているそれぞれの置換基はいずれも異なるので、中心の炭素原子は不斉中心であることが分かります。少し考えれば分かると思いますが、上記の2分子は互いに鏡写しの関係にあります。これより、乳酸分子にはエナンチオマーが存在することが分かります。
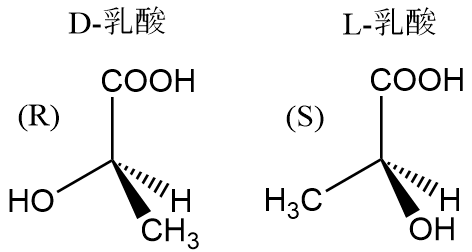
それぞれの乳酸はD体、L体と呼ばれています。余談ですが、乳酸は古くから筋肉疲労の原因物質と考えられてきました。ところが最近の研究により、寧ろ筋肉の疲労を取り除く働きがあることが分かってきています。常識と思われてきたことも数十年後には真逆の説が正しくなっていることなんてザラなんですね。
● ● ●
ところで、上記の図でRとSという文字が書いてありますが、これは一体何でしょうか?
・・・これこそがエナンチオマーを区別する重要な記号なのです。これがマスターできれば異性体の半分は攻略したも同然です!
そこでR/S表記法を学ぶ前に、CIP順位則という重要な考え方を理解しておきましょう。
✎CIP順位則とは
CIP順位則は英語で言うと “Cahn-Ingold-Prelog priority rule” となり、「CIP」という文字列はこの順位則を提案した3人の化学者の名前の頭文字を取ったものになっています。「カーン・インゴルド・プレローグ順位則」と呼ばれるこの規則はIUPAC命名法において立体配置を決定する方法として利用されています。
CIP順位則には次のようなルールがあります。
①原子番号が大きい原子の方が高順位
(同位体の場合は質量数の大きい方が高順位)
②比較している原子の順位が等しいときは、その原子に結合している次の原子の順位で更に比較する
③二重結合がある場合、二重結合している相手の元素をもう1つ加えて比較する(三重結合がある場合、三重結合している相手の元素を2つ加えて比較する)
他にも細かいルールはあるのですが、取り敢えずこの3つさえ覚えておけば困ることは滅多にありません。それでは早速、例で理解していきましょう。
● ● ●
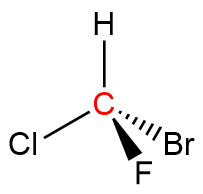 例①
例①
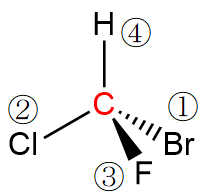
この分子では注目している炭素原子(C)にH、F、Cl、Brの各原子が結合しています。これらの原子はすべて異なるので原子番号の大きさで単純に比較できて、CIP順位則によるとH<F<Cl<Brとなりますので、CIP順位は①Br、②Cl、③F、④Hと決まります。
» 答えはこちら
» 閉じる
● ● ●
 例②
例②
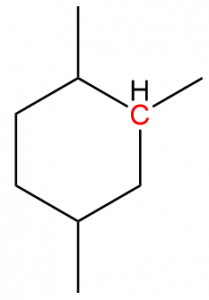
次の例です。環状分子ですが、規則通り順位付けしていきましょう。注目している炭素原子(C)には1つの水素、3つの炭素が結合しています。この時点で水素の順位は④と決まります。3つの炭素は順位が等しいので、それらに隣接して結合している原子を比較します。
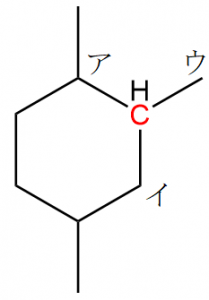
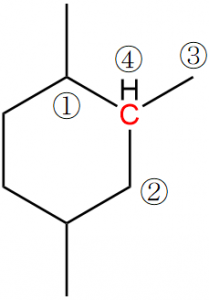
アの炭素には1つの水素と2つの炭素、イの炭素には2つの水素と1つの炭素、ウの炭素には3つの水素が結合しています。このとき、図では水素原子が省略されていることに注意しましょう。これにより、CIP順位は①ア、②イ、③ウと決まります。
» 答えはこちら
» 閉じる
● ● ●
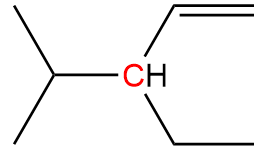 例③
例③
最後に不飽和結合が存在する分子で練習しましょう。例②のときと同様、注目している炭素原子(C)には1つの水素、3つの炭素が結合しているので水素の順位は④と決まります。問題はその次です。

アの炭素には1つの水素と2つの炭素、イの炭素には2つの水素と1つの炭素、ウの炭素には1つの水素が結合し、1つの二重結合が存在しています。CIP順位則では単結合による比較をするため、二重結合をしている相手の原子を仮想的に1つ増やすという操作をします(このようにして増えた仮想的な原子をレプリカ原子といいます)。
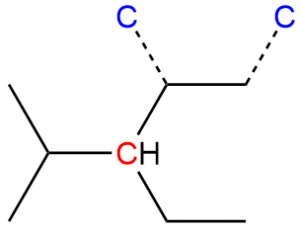
こうしてウの炭素原子には1つの水素と2つの炭素が結合していると見なすのです。ここまでの操作で炭素イの順位が③に決まります。
次に炭素アと炭素ウの比較ですが、炭素アに隣接した2つの炭素はメチル基の炭素であり、炭素ウに隣接した2つの炭素は1つはメチル基、もう一つはエチル基の炭素となっています(ここでもレプリカ炭素が順位に影響しています)。したがって順位はア<ウとなるので、①ア、②イ、③ウとCIP順位が決まります。
» 答えはこちら
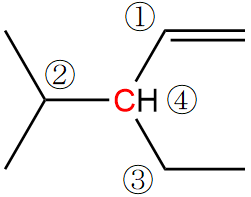
» 閉じる
● ● ●
いかがでしょうか?CIP順位則に大分慣れてきた頃かと思いますので、いよいよR/S表記法について学びましょう!
立体配置=立体配座?
皆さん何気なく有機化合物というものをイメージしているかもしれませんが、化合物には必ず立体的な描像が存在しています。
シクロヘキサンという化合物を例にとってみましょう。シクロヘキサンを紙に描いてみてください、と言われたら、皆さんはどのような構造を描くでしょうか?
ここまで勉強してきた方であれば何となく察しが付くと思いますが、シクロヘキサン分子は彫刻のようにカッチリした形をしている訳ではありません。
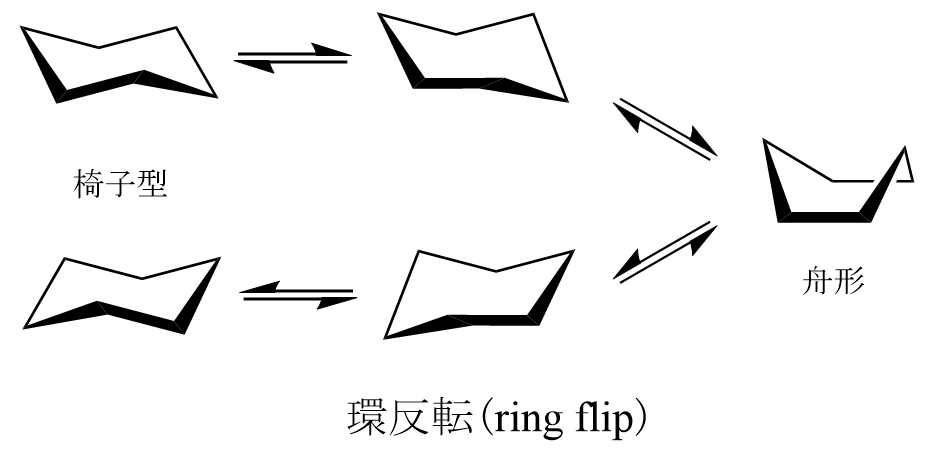
シクロヘキサン分子は上図のように絶えず環反転(ring flip)を起こしており、その実体は実にグニャグニャとしたものなのです。ときには椅子型、ときには舟型として存在しており、どれもシクロヘキサン分子であることには変わりありません。このように常温常圧など一定の条件下で分子がとりうる立体構造のパターンを「立体配座」と言います。英語では “conformation” と呼ばれ、各コンフォマーのエネルギーの高低によってそれぞれの配座がどの程度の割合で存在しているのかを速度論的に解析することができます。
これに対して、本節で学んでいる「立体配置」というのは相互に変換できないような立体的位置関係にある構造パターンを指しています。例えば冒頭で紹介したキラルな化合物は互いに変換することが困難な化合物です。言い換えると、結合を切断しなければ相互変換が不可能な立体構造のパターンを「立体配置」と呼んでいます。
皆さんの腕は伸ばしたり曲げたりすることができると思います。このように腕を伸ばした状態や広げた状態、曲げた状態などは言ってみれば立体配座(conformation)に相当しています。しかし右腕と左腕を入れ替えることはできませんよね?(これが「結合を切断しなければ相互変換が不可能」ということに相当します)このような右腕と左腕の関係性(右側に右腕が付いていて、左側に左腕が付いている、という立体構造)が立体配置に相当しています。
・・・ということで、立体配置$\ne$立体配座であることがお分かり頂けたかと思います。
✎R/S表記法をマスターする!
CIP順位則を解説しましたので、R/S表記法を学ぶためのお膳立てができました。ただしR/S表記法をマスターするには少しばかり空間把握能力が必要です。
簡単にR/S判定の手順を説明すると次のようになります。
不斉炭素の4つの置換基にCIP順位則を適用する
↓
最も低順位の置換基が奥になるように見る
↓
残りの3つの置換基の順位が時計回り順ならR体、反時計回り順ならS体とする
言葉だけでは理解が難しいと思いますので、これも具体例で確認しましょう。
次に示す分子は1‐ブロモエタノールです。1位の炭素(アスタリスクで印を付けた炭素)が不斉炭素となっており、R/S判定が可能です。
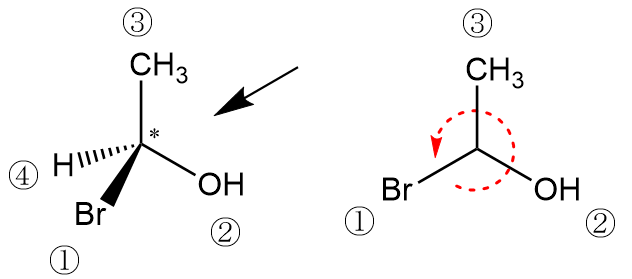
1‐ブロモエタノールの不斉炭素についてCIP順位則を適用すると左図のようになり、水素が④番目と最も低順位の置換基であることが分かります。そこで水素を奥に見ると右図のようになり、残りの3つの置換基は反時計回り順に並んでいることが分かります。したがって、この分子はS体と判断できて「(S)‐1‐ブロモエタノール」と命名することができます。
続いて2‐ブタノールを考えてみます。こちらは2位の炭素が不斉炭素となっており、エナンチオマーを区別して命名するにはやはりR/S判定が必要となります。
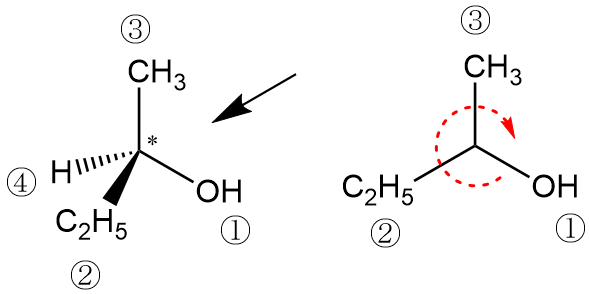
この例でも水素が最も低順位の置換基となっているので、水素を奥に見ると右図のようになり、残りの3つの置換基は時計回り順に並んでいることが分かります。したがって、この分子はR体と判断できて「(R)‐2‐ブタノール」と命名することができます。
ここではいずれの例も水素が最低順位の置換基でしたが、一般的には水素以外の置換基が最低順位となることもあります。正しくR/S判定をするためにはCIP順位則の理解が欠かせないことがお分かり頂けたかと思います。
本節ではR/S判定までの内容を中心的に扱いました。
高校の化学では「鏡像異性体」という単語を習ったかと思いますが、化学の世界では「エナンチオマー」という単語が主流です。そして立体異性体にはこの他にもう一つ重要なグループである「ジアステレオマー」が存在します。「シス体」や「トランス体」という言葉を聞いたことがあれば、それらの名が付く化合物はジアステレオマーに分類されます。
本章の冒頭で目標に掲げたアルケン化合物の命名はジアステレオマーの理解を以て完結します。という訳で、次節では残りの立体異性体であるジアステレオマーについて学び、有機化学における命名法の基礎をマスターしましょう!
