Q.
フェノール類はヒドロキシ基($\text{-OH}$)を持ちますが、アルコールに分類して良いのでしょうか?
A.
フェノール類はアルコールに分類されません。
【解説】
有機化学において「フェノール類」は芳香族環上にヒドロキシ基を持つ有機化合物を指します。ヒドロキシ基を持つためアルコールと類似した構造と言えますが、通常、フェノール類は普通アルコールには分類されません。これは、フェノール類がアルコールには見られない特徴的な性質を持つためです。(以下の解説は大学の有機化学の範囲ですが、高校生の方でも知っておくと何かと役に立つと思います)
ヒドロキシ基が芳香族の置換基であるような化合物では脱プロトン化体のアニオンが共鳴構造を取ります。
「脱プロトン化体」とは、ヒドロキシ基の水素がO-H結合を切ってプロトン(水素イオン)として脱離した構造を指します。
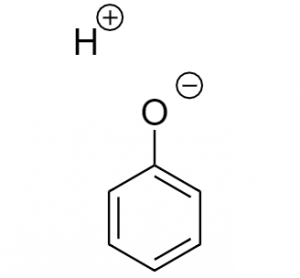 図.フェノールの脱プロトン化体
図.フェノールの脱プロトン化体
このときプロトンはカチオン(陽イオン)として出ていくので、ヒドロキシ基の部分には電子が残ります。したがって分子はアニオン(陰イオン)になります。
一般に電子が狭い空間に留まる状態はエネルギー的に不安定となるため、電子はできるだけ広い空間に分布しようとします。ベンゼン環には$\pi$軌道という広い軌道(≒電子が分布できる空間)が存在します。これにより、ヒドロキシ基の脱プロトン化により生じた電子は酸素原子上だけでなくベンゼン環の$\pi$軌道にも広がることができます。
大学レベルになりますが、フェノールアニオン(フェノラート)の共鳴構造式(極限構造式)は以下のように書くことができます。
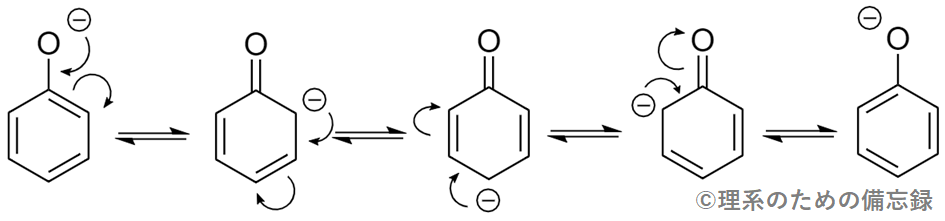 図.フェノラートの共鳴
図.フェノラートの共鳴
このように複数の共鳴構造の寄与によって電子が広い空間に分布することを「非局在化」と言います。軌道が広いほど電子のエネルギーは下がる(安定化する)ため、電子が非局在化できる構造を持つ分子はプロトンを放出しやすいと言えます。言ってみれば、電子は広いところが好きなのです。
というわけで、ベンゼン環に直接ヒドロキシ基が生えているフェノール類はアルコールに比べて酸解離定数$\text{p}K_a$が小さくなります。つまり、フェノール類はアルコールに比べて酸性度が高いという性質を持ちます。
実際、フェノールの酸解離定数$\text{p}K_a$は$9.95$ですが、飽和炭化水素にヒドロキシ基が生えているシクロヘキサノールでは約$16$です。これはシクロヘキサノールよりもフェノールの方が$10^6$倍以上も強い酸であることを意味します。
このような酸性度の高さはフェノール類に特有の性質であり、通常、フェノール類はアルコールに分類されません。
