有機化学の問題文の中で「環境が異なる炭素/水素が○○種類…」という表現が使われることがあります。初めて有機化学に触れる人にとっては「環境が異なる」という言葉の意味が分かりにくいと思いますが、意外と単純なことしか言っていません。今回はこのフレーズについて解説してみたいと思います。
「環境」って何?
まず原子にとって「環境」というものが何を意味するものなのかを押さえておく必要があります。
分子の対称性を考えたときに、他の官能基との相対的な位置関係が同じであれば「環境が同じ」と言い、相対的な位置関係が異なれば「環境が異なる」と言う。
具体的に見てみましょう。
例えばシクロヘキサンの炭素と水素はどれも互いの位置関係が同じです。このように位置を交換しても “居心地” が変わらないような原子の組を「等価」な組などと言います。
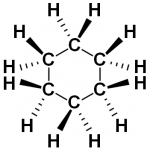 図.シクロヘキサン
図.シクロヘキサン
分子模型があればもっと分かりやすいと思います。幸い、ネットが発達した今の時代にはmolviewという優れたオンラインアプリがあります。このアプリでシクロヘキサンの立体構造を実際に眺めてみるととても参考になります。
(スワイプorドラッグすると動かせます)
では、エタノールの場合はどうでしょうか?
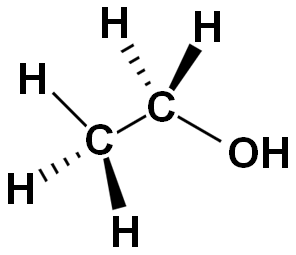 図.エタノール
図.エタノール
3Dモデルは以下のようになります。エタノールには環境の異なる炭素原子が2個存在しています。
色々動かしてみると、環境の異なる水素原子は、①ヒドロキシ基の水素1個、②真ん中の炭素原子に結合した水素2個、③末端の炭素原子に結合した水素3個、の計3種類の水素原子があることが分かります。このとき、エタノールには異なる環境の水素が3つ(3種類)存在する、などと言います。
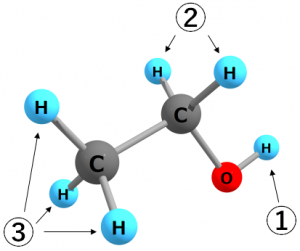 図.異なる環境の水素(3種類)
図.異なる環境の水素(3種類)
これが例えばプロパンの場合だと、異なる環境の水素は2種類だけです。端の炭素に付いている水素はどれも同じ環境と見なされます。
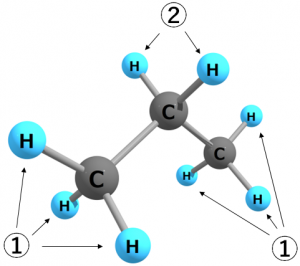 図.異なる環境の水素(2種類)
図.異なる環境の水素(2種類)
C-C単結合は自由に回転可能であるため、①とラベル付けされた末端の6個の水素原子は区別できません。したがって、プロパンの水素のうち、環境が異なるものは2種類ということになります。
「環境」と不斉炭素原子
環境の異なる炭素原子の有無は、その分子の対称性に大きく関係しています。例としてプロパノールの構造を考えてみましょう。
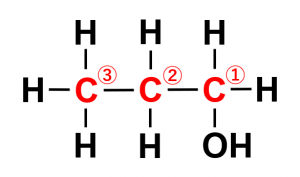 図.1-プロパノール
図.1-プロパノール
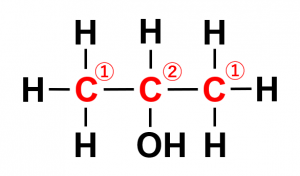 図.2-プロパノール
図.2-プロパノール
1-プロパノールでは異なる環境の炭素原子は3つ、2-プロパノールでは2つです。これは2-プロパノールの場合、中央の炭素原子を境にして対称であるため、異なる環境の炭素原子は2つになります。
 図.プロパノール (異性体2つ)
図.プロパノール (異性体2つ)
分子の対称性は不斉炭素原子の有無にも関係しています。プロパノールにメチル基が増えた2-ブタノールには異なる環境の炭素原子が4つ存在し、不斉炭素原子を持ちます。
 図.2-ブタノール
図.2-ブタノール
上の図では②の炭素が不斉炭素原子です。同じブタノールでも1-ブタノールには4つの炭素原子の環境がすべて異なる一方で、不斉炭素原子を持っていません。
分子に対称性がある場合は炭素原子や水素原子の環境が等価になる場合がある、ということを覚えておきましょう。不斉炭素原子については「【高校化学】不斉って何?不斉炭素原子とは?」のページで詳しく解説しています。
ベンゼン環の$n$置換体
芳香環における水素原子や炭素原子の環境は、化合物の構造決定の際に注目すべきポイントです。
ベンゼンの場合、6個の炭素原子の環境はいずれも等価です。
ベンゼンの1置換体
ベンゼンの1置換体の場合、異なる環境の炭素原子は4種類で、異なる環境の水素原子は3種類です。以下に水素原子を省略して炭素原子を色分けした絵を示します(Xは水素以外の原子団)。
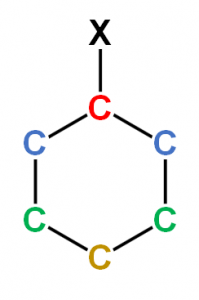 図.ベンゼンの1置換体
図.ベンゼンの1置換体
ベンゼンの2置換体
ベンゼンの2置換体の場合は、置換基の相対位置によって炭素原子の種類が変わります。同一の置換基の場合は以下のようになります(水素原子は省略)。
 図.ベンゼンの2置換体
図.ベンゼンの2置換体
(左からオルト体, メタ体, パラ体)
上の図で色分けしたように、異なる環境の炭素原子はオルト体では3種類(2種類)、メタ体では4種類(3種類)、パラ体では2種類(1種類)です(括弧内の数字は異なる環境の水素原子の種類数)。
異なる置換基による2置換体の場合は、オルト体とメタ体ではすべての炭素原子・水素原子の環境が異なり、パラ体では4種類の異なる環境の炭素原子、2種類の異なる環境の水素原子をもちます。ベンゼンの2置換体のうちパラ体は対称性が高く他の置換体と簡単に区別できるため、構造決定問題の答えになりやすいです。
ベンゼンの3置換体
ベンゼンの3置換体の場合は、置換基の相対位置によって炭素原子の種類が変わります。同一の置換基の場合は以下のようになります(水素原子は省略)。
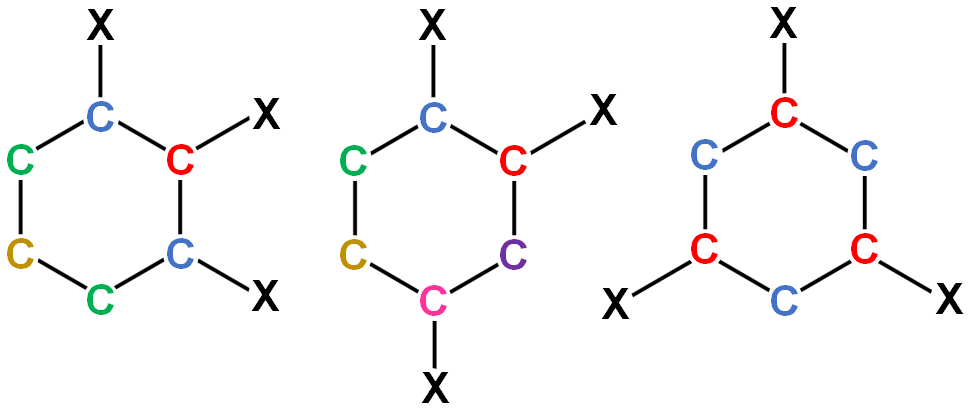 図.置換基XXXの3置換体
図.置換基XXXの3置換体
異なる環境の炭素原子は1,2,3位の置換体では4種類(2種類)、1,2,4位の置換体では6種類(3種類)、1,3,5位の置換体では2種類(1種類)です(括弧内の数字は異なる環境の水素原子の種類数)。
置換基が異なる場合は次のようにリストアップできます。
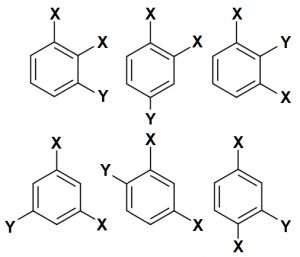 図.置換基XXYの3置換体
図.置換基XXYの3置換体
(計6パターン)
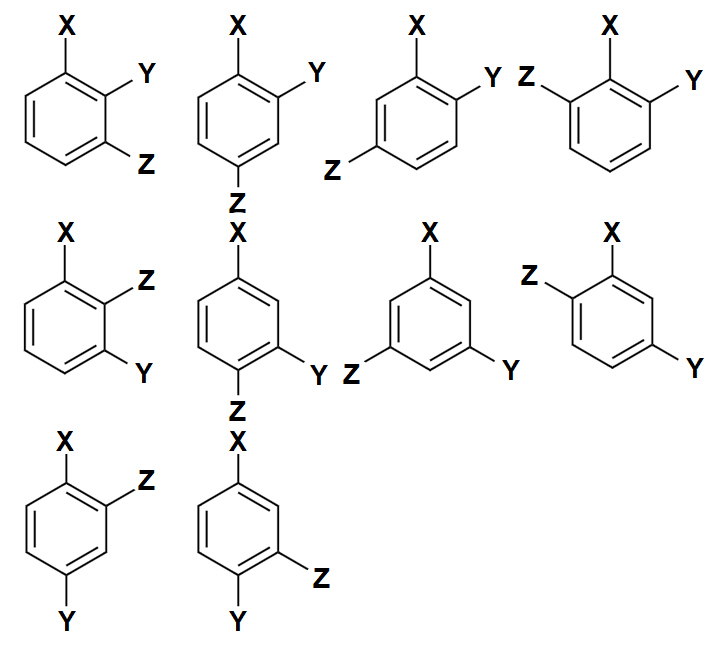 図.置換基XYZの3置換体
図.置換基XYZの3置換体
(計10パターン)
置換体の数え上げ&絞り込みはケアレスミスを防ぐためにも系統的に行いましょう。
入試問題での出題例
信州大学の2020年前期試験の大問3として、次のような問題が出題されています。
ベンゼンの一置換体$\text{C}_6\text{H}_6\text{-X}$に置換反応をさらに行う場合、置換基の種類によって次の置換反応の起こりやすい位置が決まる。たとえば、$\text{-X}$がアルキル基やヒドロキシ基である場合はオルト位とパラ位に置換反応が起こりやすく、$\text{-X}$がカルボキシ基やニトロ基である場合はメタ位に置換反応が起こりやすい。このような性質を配向性という。
常温でトルエンに①混酸(濃硝酸と濃硫酸の混合物)を加えると、構造異性体である化合物$\text{A}$および化合物$\text{B}$がおもに得られた。化合物$\text{A}$および$\text{B}$のベンゼン環の水素原子1個を塩素原子で置換すると、それぞれ化合物$\text{A}$からは4種、化合物$\text{B}$からは2種の異性体が得られる。化合物$\text{A}$にスズと濃塩酸を加え加熱すると化合物$\text{C}$が得られた。化合物$\text{C}$に水酸化ナトリウム水溶液を加えると化合物$\text{D}$が遊離した。化合物$\text{D}$を希塩酸に溶かし、氷冷しながら亜硝酸ナトリウム水溶液を加えた。その後、温度を上げると窒素および塩化水素が生じ、化合物$\text{E}$が得られた。化合物$\text{B}$に②過マンガン酸カリウム水溶液を加えて加熱した後、希硫酸を作用させると化合物$\text{F}$が得られた。
(1)化合物$\text{A}$の名称を答えよ。
(2)化合物$\text{A}$、$\text{B}$、$\text{C}$、$\text{D}$、$\text{F}$の構造式を示せ。
(3)トルエンに最初下線部②の操作を行い、次に加熱しながら下線部①の操作を行うと、1種類の生成物$\text{G}$がおもに得られた。生成物$\text{G}$の名称および構造式を示せ。
(4)【省略】
自力で解きたいという方は5分程度を目標に解いてみましょう。典型問題なので解答には10分も掛けたくありません。
以下、簡単に解説していきます。
トルエンに混酸を加えると発熱しながらベンゼン環のニトロ化が進行します。問題文中に「$\text{-X}$がアルキル基やヒドロキシ基である場合はオルト位とパラ位に置換反応が起こりやす」いとあるので、オルト位もしくはパラ位が置換されていると考えるのが妥当でしょう。
化合物$\text{A}$の構造を決めるヒントは「化合物$\text{B}$からは2種の異性体が得られる」という部分にあります。化合物$\text{A}$と$\text{B}$は異性体なので組成式は共通です。化合物$\text{B}$のベンゼン環の水素原子1個を塩素原子で置換すると2種の異性体が得られる、というのは即ち、化合物$\text{B}$のベンゼン環における環境の異なる水素原子は2種である、ということを言っています。
ベンゼンの2置換体のうちでパラ体のみが2種類の異なる環境の水素原子を持つことを思い出すと、化合物$\text{B}$はパラ体の構造だと分かります。このとき3置換体の可能性を考えた人がいたかもしれませんが、「異なる環境の水素原子が2つ」というのはパラ体(2置換体)に特有の性質であるため、化合物$\text{A}$と$\text{B}$は(メチル基とニトロ基の)2置換体で確定です。
以上の考察により、化合物$\text{B}$がパラ体(p-ニトロトルエン)、化合物$\text{A}$はオルト体(o-ニトロトルエン)と判明します。
それ以降の問題文はo-トルイジンを経由したo-クレゾールの製法についての記述で、基本的なフェノール化反応(ニトロ化→還元してアミノ化→亜硝酸ナトリウムでジアゾ化→加熱による脱窒反応)に習熟していれば容易に処理できる紋切り型の問題です。確実に得点しましょう。
因みに、下線部②の操作はベンゼン環に生えているアルキル基の酸化反応であり、この後に希硫酸を作用して遊離する酸はメチル基がカルボキシ基に変換された構造になります。したがって、化合物$\text{F}$はp-ニトロ安息香酸と分かります。これと(3)はアルキル基の酸化反応に関する知識が無いと解けなかったかもしれませんね。
【発展編】その他の特殊な場合
以下は高校化学の範囲を逸脱する内容なので、高校生・受験生の方はスルーして頂いて構いません。
原子の置かれている環境が異なる条件は対称性だけに留まりません。例えば、C-C結合は自由に回転可能ですが、立体障害など何らかの理由で回転が阻害されている場合は事実上の構造異性体が発生します。これを軸不斉と呼びます。このような不斉を持つものはアトロプ異性体と呼ばれています。
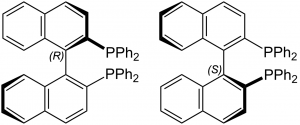 図.軸不斉を持つ例:BINAP分子
図.軸不斉を持つ例:BINAP分子
また、分子の対称性は平面的なものに限りません。一般に有機化合物は3次元的な構造を持ち、立体的な対称性というものも考えられます。例えば最も単純なカゴ型分子であるアダマンタン (adamantane) は以下のような構造をしています。
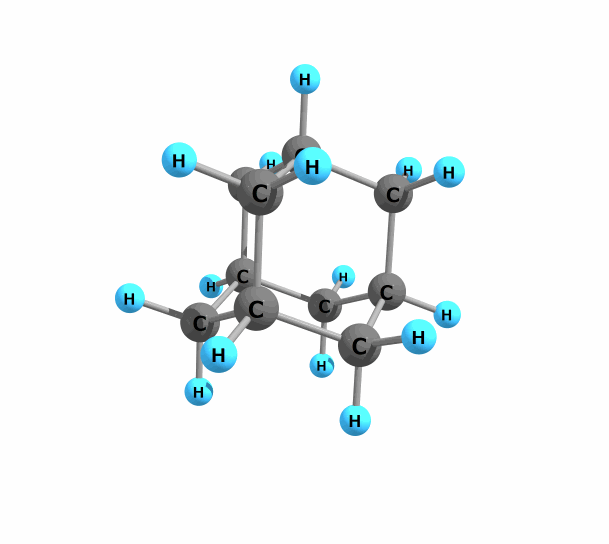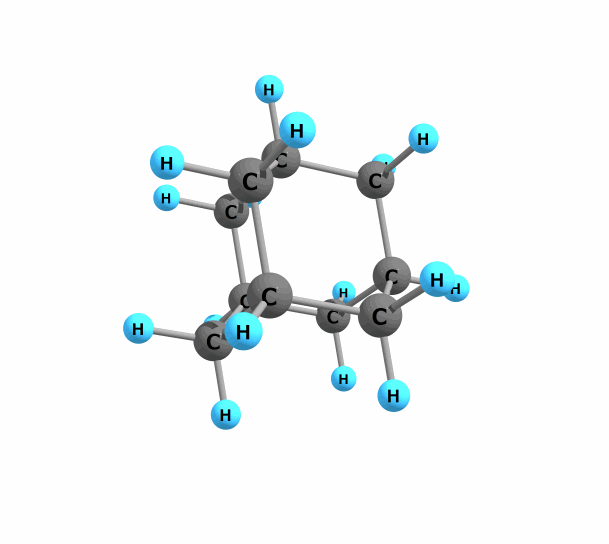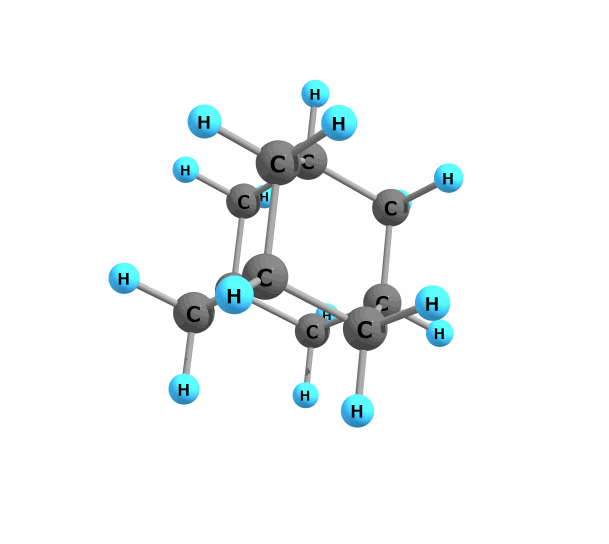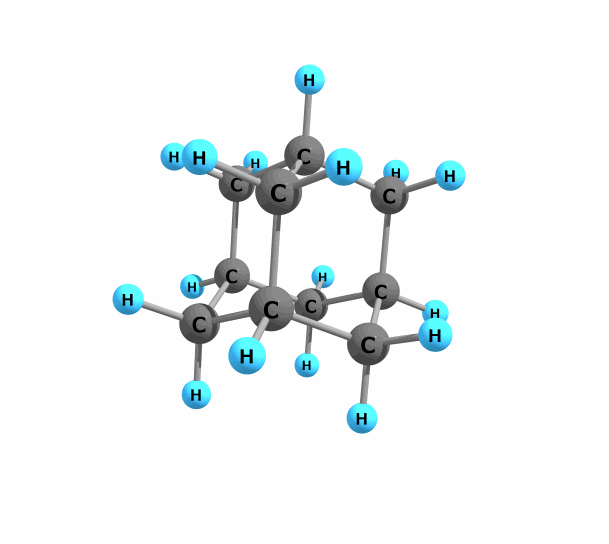 図.アダマンタン
図.アダマンタン
アダマンタンは非常に対称性が高く精密にパッキングするため、分子性結晶構造が非常に安定であり融点は270°Cと有機化合物にしてはかなり高温です。分子内の炭素原子・水素原子の環境はともに2種類に分けられるので、確かめてみて下さい。
(2021/10/18追記)本文の表現を一部変更、目次の追加

大学の化学では群論を使ってもっと一般的に分子の対称性を議論します。環境の異なる水素(プロトン)の数によってNMR測定の結果が変わるので、原子の「環境」は有機化合物の高度な構造決定において重要なヒントになります。